לחתוך החוצה את תסמונת דאון
חוקרים הראו – בינתיים רק בתרבית – שאפשר לכאורה לתקן את התסמונת הגנטית הנפוצה, הנובעת מעותק מיותר של כרומוזום 21 בגרעין התא
לבני אדם יש 23 זוגות כרומוזומים, כלומר 46 בסך הכול. בתאי המין שלנו – ביציות ותאי זרע – יש בדרך כלל רק עותק אחד של כל כרומוזום, כך שכשמתרחשת הפריה והזרע והביצית מתאחדים לתא עוברי אחד, הצאצא מקבל שני עותקים של כל כרומוזום, אחד מכל הורה.
לעיתים מתרחשת תקלה בהפרדת הכרומוזומים במהלך יצירת תא מין, ושני כרומוזומים מאותו סוג נשארים יחד. כשמתרחשת הפריה והתא הפגום מתאחד עם תא מין מההורה השני, ייווצר עובר עם עודף בכרומוזום מסוים. מצב כזה קרוי גם טריזומיה, כלומר מצב של שלושה כרומוזומים מאותו סוג. מה שיקרה לאחר מכן תלוי בסוג הכרומוזום העודף. חלקם פשוט לא ישלימו את ההיריון. אחרים יסתיימו בלידה, אך התינוק עלול לסבול מבעיות בהתפתחות או ממומים אחרים.
תסמונת דאון היא התוצאה של תקלה בחלוקת כרומוזום 21 לפני ההפריה, כך שבביצית המופרית יש שלושה עותקים של הכרומוזום. לילדים עם התסמונת יש מבנה פנים אופייני, שכולל עיניים מלוכסנות מעט ולשון מעובה, ושורה ארוכה של תסמינים שעשויים לכלול פיגור שכלי, עיכוב התפתחותי, איחור ברכישת השפה, נטייה למומי לב, לבעיות במערכת העיכול ובמערכת החיסון ועוד. אפשר לאבחן את התסמונת בשלב מוקדם של ההיריון, בבדיקות סקר מוקדמות שיאפשרו להורים לבחור אם לסיים את ההיריון או לשמור אותו.
נכון לעכשיו אין דרך למנוע את התפתחות התסמונת או לרפא אותה. מחקר חדש מציע שיטה לסלק את הכרומוזום המיותר בכלים של הנדסה גנטית, בתקווה שבעתיד היא תבשיל לטיפול יעיל שיתקן את מבנה הכרומוזומים בתאים ויבטל את הטריזומיה.
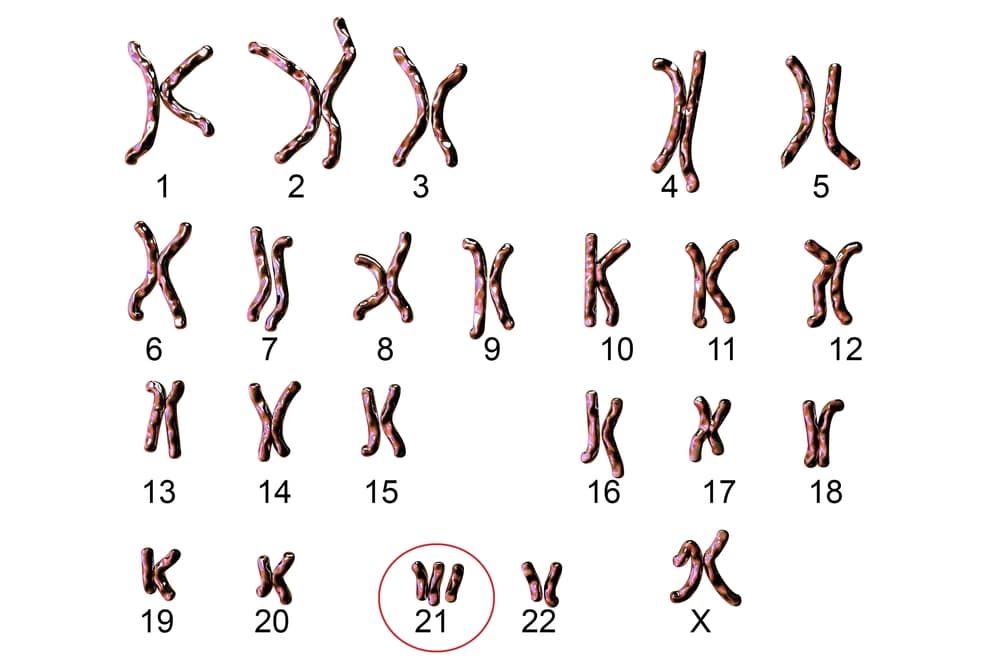
טריזומיה של כרומוזום 21 שגורמת לתסמונת דאון. 22 כרומוזומים תקינים וכרומוזום 21 עם שלושה עותקים (מוקף בעיגול) | Kateryna Kon, Shutterstock
המספריים של קריספר
במחקר, שנערך ביפן ופורסם בכתב העת PNAS Nexus, בחנו החוקרים את האפשרות להשתמש במערכת קריספר כדי להשמיד את הכרומוזום העודף. קריספר היא טכנולוגיה לעריכה גנטית שמאפשרת לחתוך מולקולות DNA במקומות ספציפיים שנבחרו מראש. החוקרים יצרו תאי גזע עם טריזומיה, שיש בהם שלושה עותקים של כרומוזום 21, שניים מהאם ואחד מהאב. הם ריצפו את סדר הבסיסים – אבני הבניין של מולקולת ה-DNA – בכל אחד מהם ומיפו את המקומות שבהם לכל כרומוזום יש מבנה ייחודי משלו.
לאחר מכן הם בחרו באחד משני הכרומוזומים שהגיעו מהאם כמטרה להשמדה, ומצאו לאורכו כ-15.7 אלף מקומות שבהם סדר הבסיסים היה ייחודי. מתוכם הם בחרו 56 אתרים מבטיחים, ואחרי בדיקות מעמיקות נותרו 13 אתרים שבהם מערכת קריספר חותכת רק את הכרומוזום המיועד להשמדה ולא פוגעת בשני האחרים, או בכרומוזומים האחרים שבגרעין התא. כשהפעילו את המערכת בתרבית תאים, 13.1 אחוז מהתאים איבדו את הכרומוזום העודף ונותרו עם זוג כרומוזומים תקין. יעילות דומה נמצאה גם בתרבית של פיברובלסטים – תאים של רקמת חיבור.
בכל התאים בגוף האנושי יש מערכות שתפקידן לתקן נזקים ל-DNA, והן יודעות לתקן גם את חיתוכי ה-DNA שמבצע מנגנון קריספר. אולם המערכות האלה אינן מושלמות, ולא פעם הן מכניסות שגיאות (מוטציות) ברצף ה-DNA באזור התיקון. התברר שבתאים שנותרו עם שלושה כרומוזומים מספר 21 נמצאו שינויים באתרים המיועדים לחיתוך, דבר שמעיד שמערכת קריספר אכן חתכה את הכרומוזום כפי שהייתה אמורה לעשות, אך מנגנוני התא הצליחו לתקן את הנזק.
על מנת לנסות ולשפר את היעילות של פירוק הכרומוזום העודף, וכדי למנוע היווצרות של שינויים גנטיים לא רצויים, החוקרים חזרו על הניסוי, אבל הפעם פגעו באופן זמני במערכת תיקון ה-DNA בתאים. בעקבות זאת, יעילות פירוק הכרומוזום העודף עלתה לכ-18 אחוז.
ניתוח של ביטוי הגֵנים בתאים, כלומר מהם הגֵנים שפעילים בכל תא, הראה שבתאים המתוקנים, שהכרומוזום המיותר שלהם הושמד, דפוסי הפעלת הגֵנים חזרו להיות דומים לאלה של תאים רגילים, ובכלל זה גֵנים שקשורים להתפתחות מערכת העצבים ועשויים להשפיע על היכולת השכלית ועל צורת הגולגולת הייחודית של בעלי תסמונת דאון. בנוסף חל שיפור בקצב החלוקה של התאים, כך שמחזור התא התקצר מ-17 שעות ל-15 שעות, בדומה לתאים בריאים.
שיפור ניכר גם בפעילות אברוני המיטוכונדריה שמייצרים אנרגיה עבור התא. בתאים עם כרומוזום עודף, תפקוד המיטוכונדריה פגום והתוצרים שלהם יוצרים נזקי חמצון בתא. בתאים המתוקנים רמת המולקולות המחמצנות ירדה בצורה משמעותית, לרמה הדומה לזו של תאים בריאים, ואף נמוכה יותר.
למרות הממצאים המעודדים, נותרה עדיין דרך ארוכה לפני שנוכל לתקן עוברים עם תסמונת דאון. המחקר הנוכחי בחן רק שני סוגי תאים, ויש לבדוק סוגי תאים רבים נוספים. אחד האתגרים הגדולים יהיה להחדיר את מנגנון הקריספר לתאי העצב ולרקמות התומכות בהם, ולראות אם חיתוך הכרומוזום העודף יתבצע שם ביעילות דומה. בנוסף, יעילות הטיפול עדיין נמוכה למדי, ויש סכנה ממשית להיווצרות פגמים בכרומוזום שהיה אמור לעבור פירוק ובכרומוזומים אחרים.
כמו כן, למרות השיפור בבריאות התאים אחרי פירוק הכרומוזום המיותר, לא ברור אם די בזה כדי לשפר את בריאותם ותפקודם של בעלי תסמונת דאון. המאפיינים הגופניים של התסמונת ניכרים כבר במהלך ההיריון, וקשה להניח שפירוק הכרומוזום העודף אחרי הלידה יוכל לתקן אותם. גם לא ברור אם העיכוב ההתפתחותי האופייני לתסמונת יושפע מטיפול אחרי הלידה, או בגיל מבוגר יותר.החוקרים מקווים שמחקרים נוספים יצביעו על הדרך הנכונה לריפוי מעשי של תסמונת דאון.



