بفضل أحد العلاجات الرّائدة، اِستغنت شابّة تبلغ من العمر 25 عامًا من تيانجين، الصّين، كانت تعاني من مرض السّكّري النّوع الأوّل، عن العلاج بالأدوية. إذ زُرعت خلايا معدّلة في جسد المريضة، ممّا مكّنها من إنتاج الأنسولين عند الحاجة. وكانت هذه المرّة الأولى الّتي ينجح فيها إجراء من هذا النّوع.
في السّكّري من النّوع الأوّل، يقوم الجهاز المناعيّ بمهاجمة خلايا الأنسولين في البنكرياس (جزر لانغرهانس)، لذلك لا تستطيع أجساد المرضى إنتاج هذا الهرمون، وبدلًا من ذلك يلجؤون إلى حقن الأنسولين بشكل دائم. في حالاتٍ محدّدة، من الممكن زراعة خلايا منتجة للأنسولين في أجسام المرضى، ولكن ترافق هذا الإجراء تحدّياتٍ عدّة، منها: قوائم انتظار المتبرّعين الطّويلة، والحاجة الى استخدام أدويّة تثبيط المناعة الّتي تمنع رفض الجسم للخلايا المزروعة. في هذا السّياق، توفّر تقنيّة زراعة الخلايا الجذعيّة بديلًا واعدًا، إذ تتيح إنتاج مصدر غير محدود من خلايا البنكرياس المُستخرجة من أجساد المرضى، ممّا قد يُسهم في توفير علاج فوريّ دون الحاجة إلى فترات انتظار طويلة، أو الاعتماد المستمرّ على أدوية تثبيط المناعة.
قام فريق بحثيّ من جامعة نانآكي، بالتّعاون والاستناد إلى نتائج سابقة لباحثين من جامعة بكّين، باستخلاص خلايا من ثلاثة أشخاص مصابين بالسّكّري من النّوع الأول، وتحفيزها للدّخول في الحالة متعدّدة القدرات (pluripotent state)- الّتي تتيح لها التّمايز لأنواعٍ مختلفة (تتغيّر لنوع آخر) من الخلايا. تمّ الاستعانة بجزيئات عضويّة صغيرة من أجل تحفيز هذه الخلايا على التّحوّر للجينات المطلوبة، حيث تتميّز هذه الجزيئات بسهولة إنتاجها، ممّا قد يتيح المجال مستقبلًا لاستخدامها كأساس لمعالجة أمراض مختلفة. في هذا البحث، تمّ تطوير الخلايا متعدّدة القدرات إلى مجموعات من خلايا البنكرياس القادرة على إنتاج الإنسولين.
بعد سلسلة من التّجارب النّاجحة على النّماذج الحيوانيّة، في يونيو 2023 قام الباحثون بإجراء تجربة، تمّ فيها زراعة حوالي 1.5 مليون خليّة أنسولين في عضلات بطن المريضة. تمّ اختيار عضلات البطن بدلًا من الكبد، الّذي كان في الماضي منطقة الزّراعة الأكثر شيوعًا، وذلك من أجل تمكين المتابعة غير الجراحيّة عبر التّصوير بالرّنين المغناطيسيّ (MRI)، بالإضافة إلى إتاحة الإمكانيّة لإزالة التّكتّلات عند الحاجة.
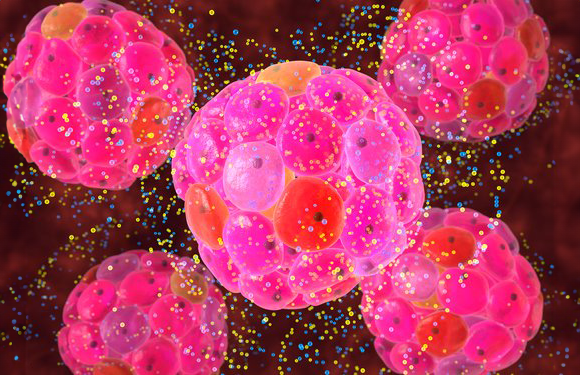
في مرض السّكّري من النّوع الأوّل، يهاجم جهاز المناعة خلايا الأنسولين في البنكرياس، ممّا يمنع الجسم من إنتاج الأنسولين، وبالتالي يحتاج المرضى إلى حقن الهرمون بانتظام. رسم توضيحيّ للخلايا المنتجة للأنسولين | Animated Healthcare Ltd / Science Photo Library
هل تغيّرت قواعد اللّعبة؟
بعد نحو شهرين ونصف من الزّراعة، بدأت المريضة في إنتاج كمّيّة كافية من الأنسولين مكّنتها من التّوقّف تمامًا عن تلقّي الأدوية الخارجيّة. على مدار أكثر من عام، بقيت مستويات السّكّر في دم المتعالجة ضمن المعدّل المطلوب لأكثر من 98% من الوقت، دون الحاجة إلى حقن الأنسولين من مصدر خارجيّ. على إثر ذلك، أشادَ الخبراء ومن بينهم الجرّاح، جيمس شابيرو من جامعة ألبرتا، بهذا الإنجاز واعتبروه نجاحًا كبيرًا.
لم يتمكّن البحث من تحديد تأثير زراعة الخلايا الجذعيّة على استجابة الجهاز المناعيّ في رفض الخلايا المزروعة، وذلك نظرًا لخضوع المريضة مسبقًا لعلاجات مثبطة للمناعة بسبب عمليّة زراعة كبد سابقة، والّتي تتطلّب علاجًا لمنع رفض الجسم للعضو المزروع. ومع ذلك، أعرب الباحثون عن تفاؤلهم تجاه هذا الإجراء، واعتقدوا أنّ الخلايا المأخوذة من المريض نفسه قد تساعد في تقليل مشكلات الاستجابة المناعيّة. بالإضافة إلى ذلك، يعمل الفريق على تطوير خلايا بنكرياسيّة مقاومة لهجمات الجهاز المناعيّ، حيث يُعدّ هذا التّحدّي إحدى المشكلات الرّئيسيّة في مرض السّكّري من النّوع الأوّل.
ينضمّ هذا البحث إلى سلسلة من الجهود المكثّفة الّتي تسعى لاستخدام الخلايا الجذعيّة في علاج مرض السّكّري. في دراسةٍ أخرى، أعلن باحثون من شنغهاي مؤخّرًا عن زراعة خلايا أُعيدت برمجتها داخل كبد رجل يبلغ من العمر 59 عامًا مصابٍ بالسّكّري من النّوع الثّاني، وبذلك توقّف المريض عن تلقّي الأنسولين من مصادر خارجيّة.
تشكّل هذه الإنجازات خطوات واعدة في علاج مرض السّكّري، إذ توفّر علاجات أكثر فعاليّة من العلاجات التّقليديّة. وفي حال استمرّت هذه التّجارب بتحقيق نجاحات مماثلة، فإنّها قد تفتح آفاقًا جديدة في علاج المرض، وسوف تضع حدًّا لاستخدام الأدوية الخارجيّة، وبالتّالي الإسهام في تحسين جودة حياة ملايين المرضى.

